
国内第Ⅲ相試験のHERB-DH1は、390例の本態性高血圧患者を対象とした、標準治療に治療用医療機器プログラムを追加した際の安全性及び有効性を評価する多施設共同無作為化比較試験です。
本態性高血圧患者のうち、降圧薬による内服治療を受けていない患者を対象に、アプリ介入群と対照群において、治験登録12週時における有効性及び安全性の比較検討を行いました。
※承認時評価資料(同データは、Kario K et al. Eur Heart J. 2021;42(40):4111-4122.にも掲載・公表されております)
国内第Ⅲ相試験HERB-DH1徹底解説
対象患者
本態性高血圧患者のうち、食事・運動療法などの生活習慣の修正を行うことで降圧効果を十分に期待できると医師が判断した者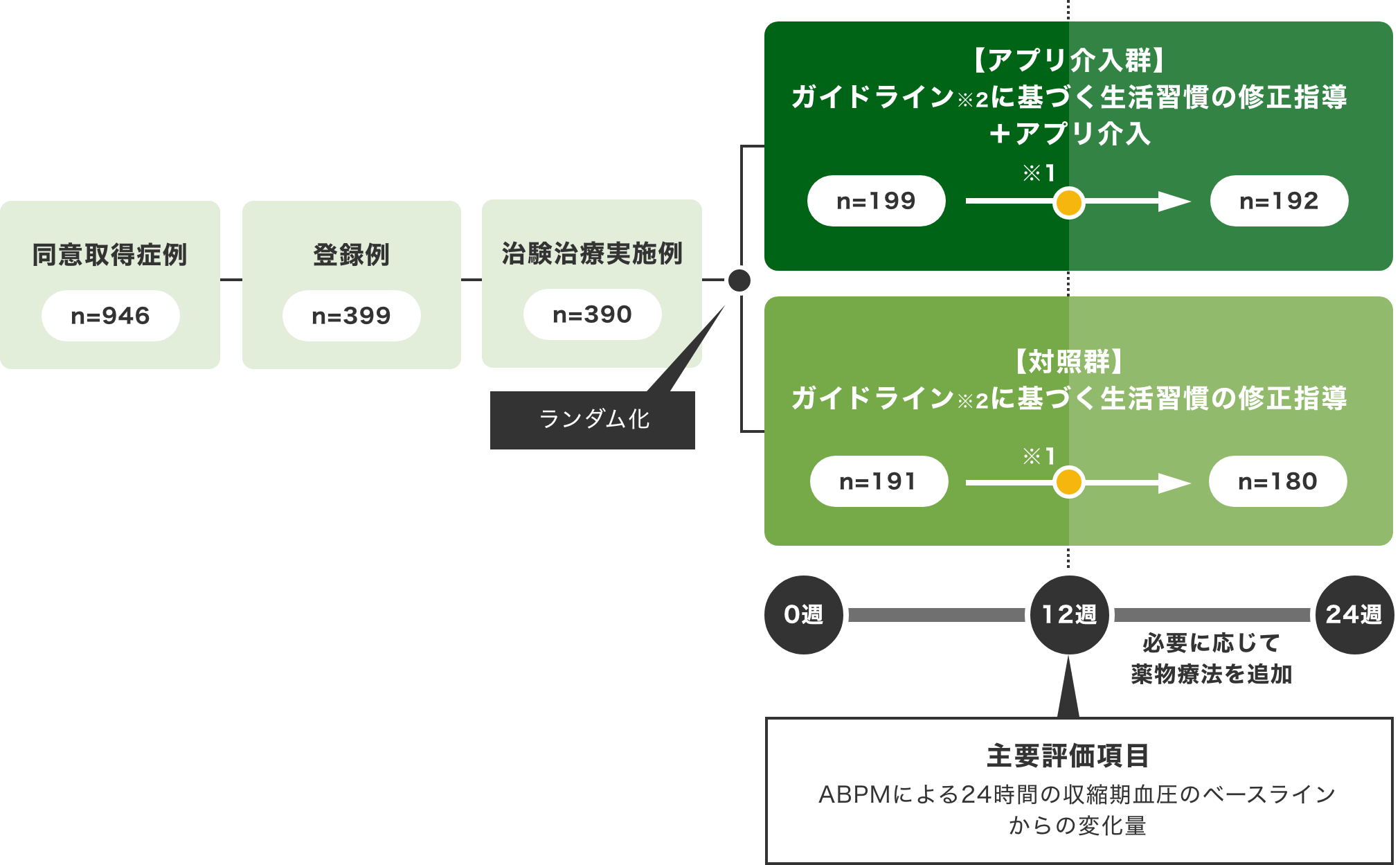
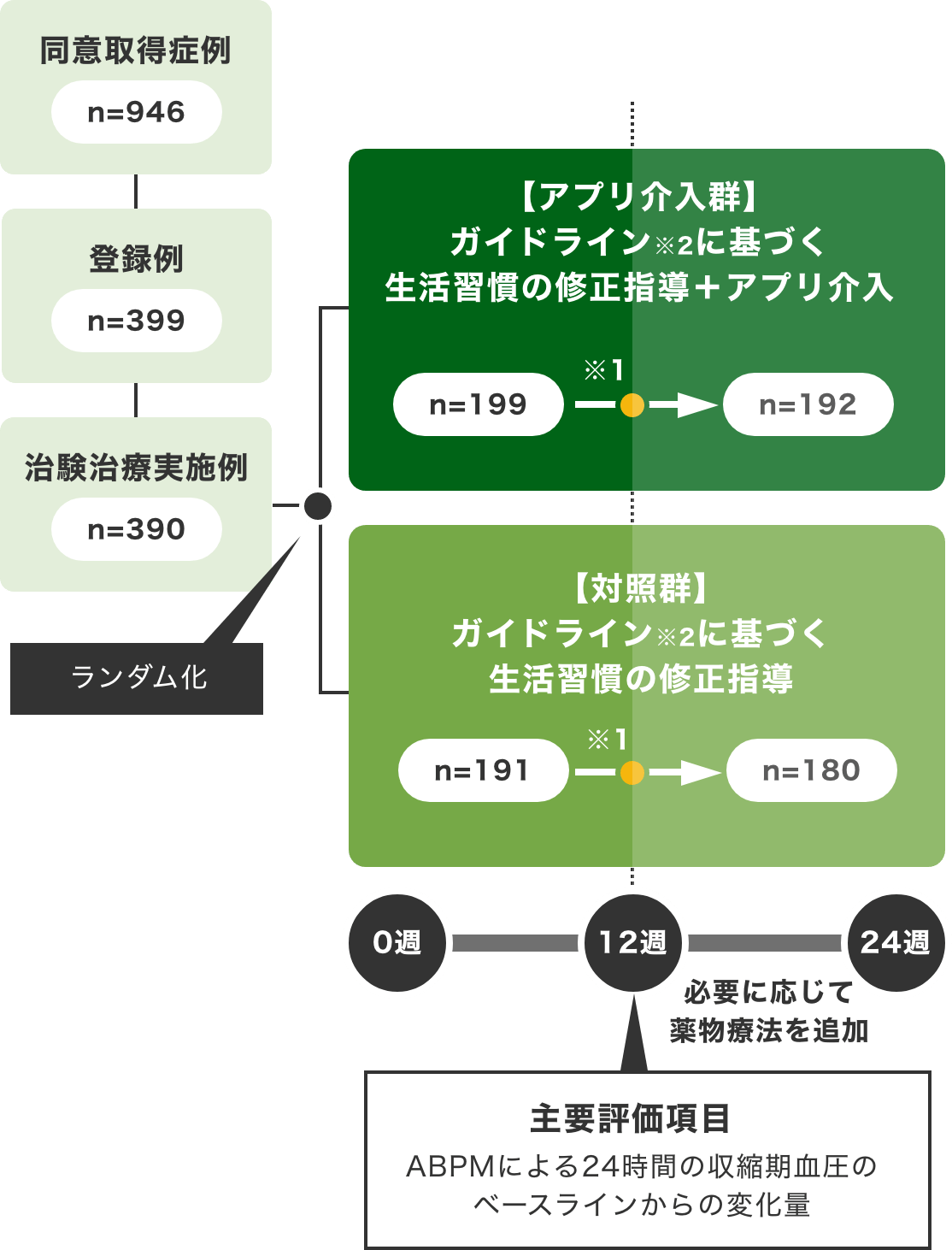
ABPM (Ambulatory blood pressure monitoring) : 自由行動下血圧測定
※1 治験登録後12週時点で薬物療法の必要性を評価し、24週後までフォローアップした
※2 高血圧治療ガイドライン2019(日本高血圧学会)
評価項目
解析計画
第一種の過誤(α=0.05)、検出力90%を考慮した上で、本治験における例数を設定した。
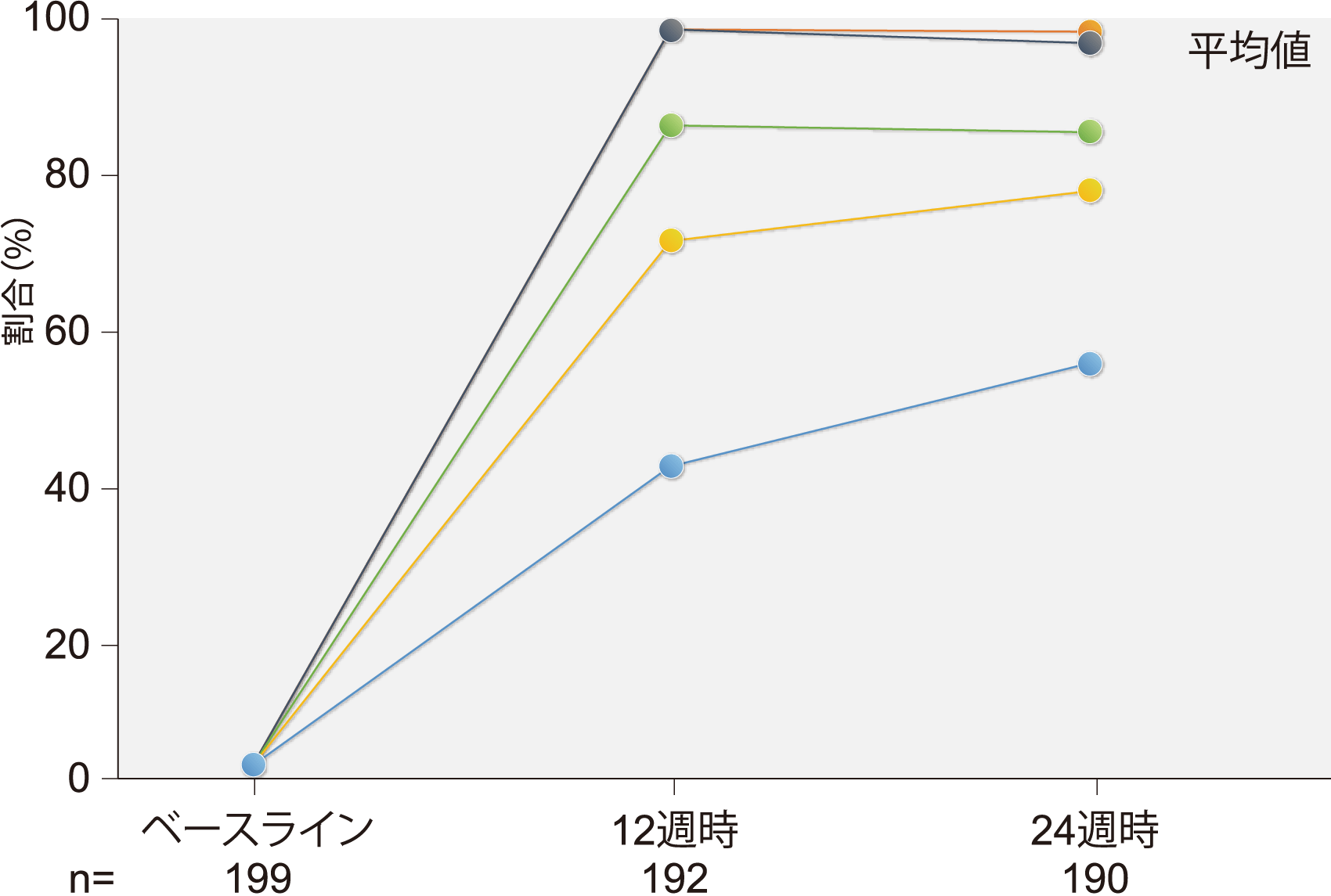
血圧値(ABPM及び家庭血圧)は、FASを対象としてアプリ介入群/対照群別、施設、薬物治療歴の有無を因子とし、ベースライン時点の血圧値を共変量とした共分散分析を用いて解析した。
その他の評価項目(体重、BMI及び塩分チェックシートによる点数のベースラインからの変化量)は、対応のないt検定を用いて解析した。
| アプリ介入群 (n=199) |
対照群 (n=191) |
||
| 年齢(歳) | 平均(標準偏差) | 52.4(8.06) | 52.0(7.59) |
| 中央値 (最小値, 最大値) |
54(21,64) | 52(22,64) | |
| 性別 | 女性 | 35(17.6%) | 43(22.5%) |
| 男性 | 164(82.4%) | 148(77.5%) | |
| 喫煙歴 | なし | 166(83.4%) | 162(84.8%) |
| あり | 33(16.6%) | 29(15.2%) | |
| 体重(kg) | 平均(標準偏差) | 73.27(13.754) | 72.95(13.301) |
| BMI(kg/㎡) | 平均(標準偏差) | 25.73(4.065) | 25.76(3.946) |
| 腹囲(cm) | 平均(標準偏差) | 88.86(10.62) | 89.34(10.49) |
| ABPMによる24時間血圧 平均(標準偏差) |
収縮期血圧 | 144.3(10.43) | 144.9(10.44) |
| 拡張期血圧 | 94.3(7.15) | 95.0(8.22) | |
| 起床時家庭血圧 平均(標準偏差) ※アプリ介入群:n=167 対照群:n=158 |
収縮期血圧 | 147.0(13.31) | 149.3(12.35) |
| 拡張期血圧 | 94.0(9.86) | 95.7(8.73) | |
| 診察室安静座位血圧 平均(標準偏差) |
収縮期血圧 | 153.2(10.51) | 154.1(10.02) |
| 拡張期血圧 | 97.9(6.93) | 98.8(7.16) | |




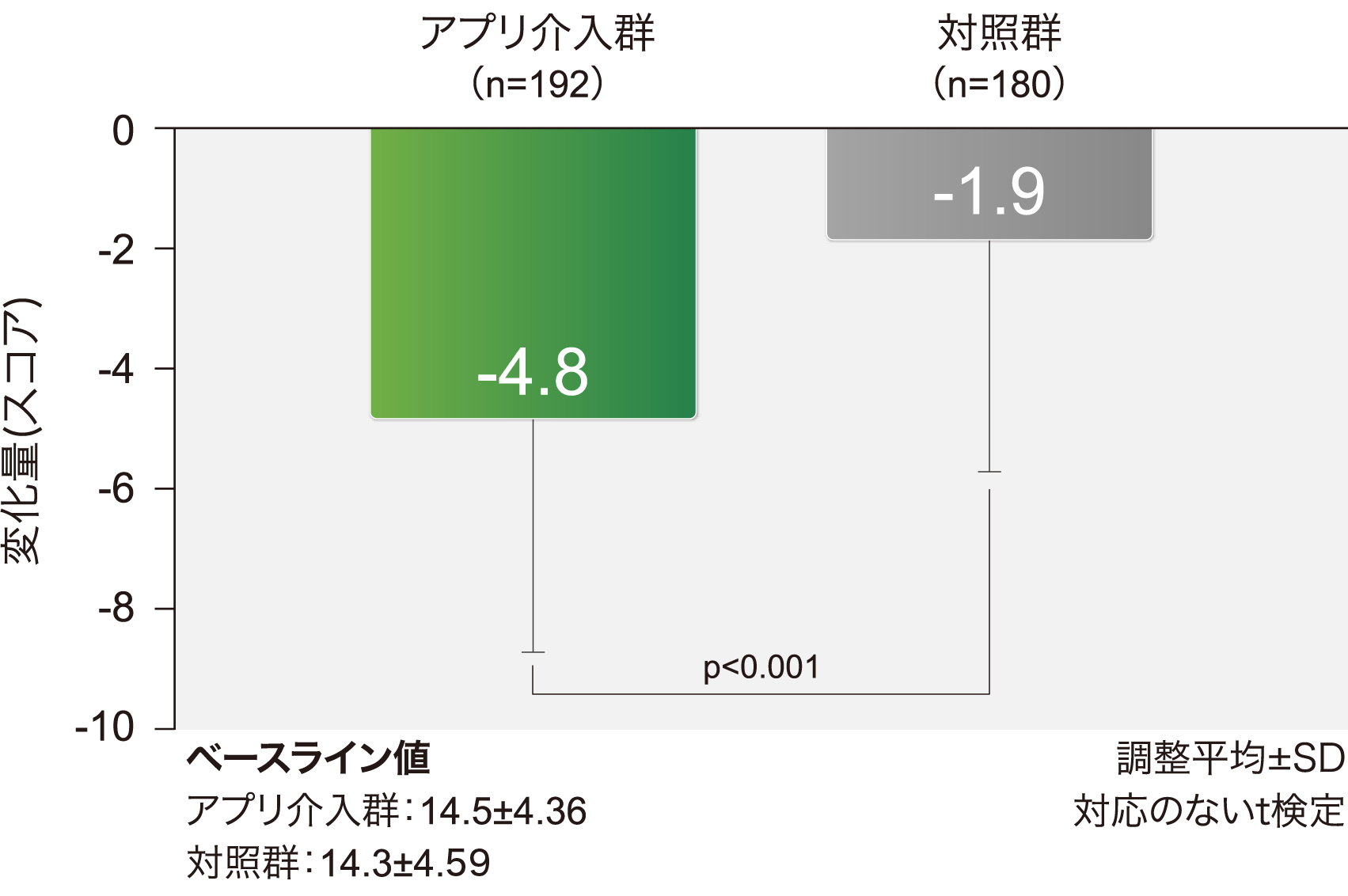
塩分チェックシートとは
高塩分食品の摂取頻度、食に関する行動、食に関する意識についての患者さんの回答をもとに食塩摂取量を点数化し、合計点で食塩摂取状況を判定する。
土橋卓也 他. 血圧. 2013;20: 1239-1243.
yasutake K et al. Hypertens. Res., 2016; 39: 879-885.
監修:製鉄記念八幡病院 理事長 土橋卓也 先生
安全性について
有害事象
すべての有害事象について、本アプリとの因果関係は否定されました。本アプリの不具合
登録後12週までに21.0%(42/200例、47件)、24週までに24.0%(48/200例、57件)で不具合が認められました。※治験時はBluetooth機能を用いてスマートフォンと家庭血圧計を接続する治験手順を設けておりましたが、実際にご使用いただく際は必須ではありません。BluetoothはBluetooth SIG, Incの登録商標です。